施李杨课题组《Materials Today Bio》:双药序贯治疗重塑脊髓损伤免疫微环境
脊髓损伤(Spinal Cord Injury, SCI)是一种严重的中枢神经系统疾病,常导致损伤平面以下感觉与运动功能的永久性丧失。其复杂的病理过程涉及炎症反应、细胞坏死、胶质瘢痕形成及再生受限等多环节。其中,小胶质细胞/巨噬细胞的极化状态在损伤进展中呈现显著的时序性动态变化:在急性期,这些细胞主要表现为促炎性的M1型表型,释放多种细胞因子,加剧组织损伤;而在损伤后期,部分细胞可转化为具有修复作用的M2型表型,但数量有限,难以实现有效的组织再生。因此,如何实现对小胶质细胞/巨噬细胞极化过程的程序化调控,是促进脊髓修复与功能恢复的关键科学问题。然而,传统治疗策略往往难以精准匹配这一时序性免疫过程。
针对上述挑战,施李杨教授团队创新性地构建了一种基于水凝胶的双药序贯释放体系,通过程序化调控药物释放,实现对小胶质细胞/巨噬细胞M1/M2极化的精准时序调节。该体系以透明质酸(HA)水凝胶为骨架,集成两种不同释放机制:在脊髓损伤急性期,利用负载于纳米颗粒中的盐酸米诺环素(Minocycline Hydrochloride, MH)快速释放以抑制M1型促炎反应;在慢性期,则通过生物素–链霉亲和素(Biotin–Streptavidin)相互作用实现白细胞介素-4(Interleukin-4, IL-4)的持续缓释,诱导M2型抗炎表型形成,从而系统性地重塑损伤区域的免疫微环境。
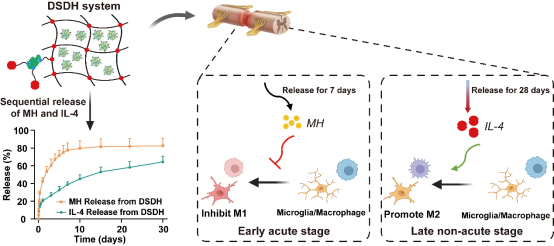
图1 双药物序贯治疗平台精准调控小胶质细胞/巨噬细胞M1/M2极化示意图
研究结果表明,该序贯治疗体系在时序性免疫调控和功能修复方面均展现出显著优势。在损伤后第7天,水凝胶有效抑制了M1型标志物iNOS的表达;至第28天,显著提升了M2型标志物CD206的水平,成功实现了从早期抑炎到后期促修复的免疫转变。功能学评估显示,经双药序贯水凝胶治疗的大鼠,其后肢运动功能(BBB评分)、步态协调性及运动诱发电位信号均明显改善。同时,该策略有效缓解了脊髓损伤常见并发症——膀胱功能障碍,显著减少了损伤区空腔形成与胶质瘢痕生成,并促进了神经元标志物Tuj-1的表达和神经纤维再生。
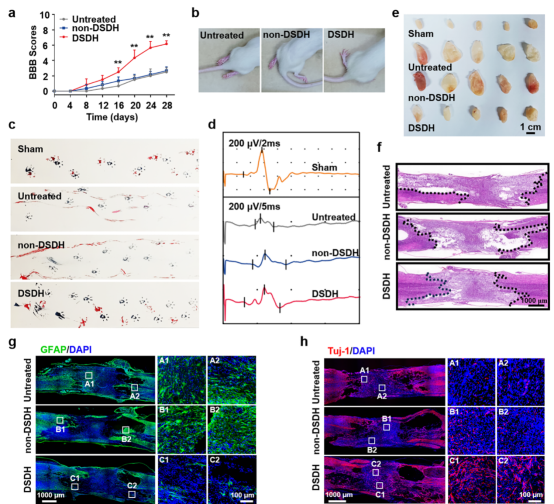
图2 双药物序贯治疗策略促脊髓损伤修复
该研究成功开发了一种可实现程序化免疫调控的双药序贯递送平台,突破了传统给药策略在时序控制上的局限,为脊髓损伤及其他神经炎症性疾病的治疗提供了新的理论基础与具有转化潜力的治疗策略。相关成果以题为“A dual-drug sequential delivery hydrogel for programmatic microglia/macrophage polarization and function recovery in spinal cord injury” 发表在《Materials Today Bio》(中科院医学类一区,IF=10.2)上(论文链接:https://doi.org/10.1016/j.mtbio.2025.102365)。湖南大学生物学院已毕业博士生李亚和在读博士生梁钰昀为论文共同第一作者,施李杨教授为通讯作者。
