慢性肾病(Chronic Kidney Disease,CKD)是全球重要的公共健康问题,其主要特征为肾功能进行性下降、肾组织持续性损伤以及毒性代谢产物在体内蓄积。CKD 的发生发展常伴随肾小管损伤、炎症反应及纤维化等病理过程,并逐步导致肾结构和功能不可逆改变。近年来研究表明,CKD 并非单一器官疾病,而是涉及多器官协同失衡的系统性疾病,其中肝脏与肾脏在毒素生成与清除过程中的代谢互作尤为关键。然而,调控肝肾互作并驱动肾损伤进展的分子机制仍有待阐明。
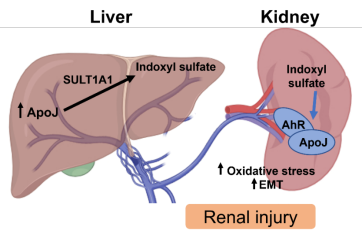
针对这一问题,孙宏羽/施李杨团队发现,ApoJ 通过介导肝肾轴双向调控,直接驱动 CKD 的发生发展。研究表明,ApoJ 在肾小管中异常蓄积,可抑制芳香烃受体(Aryl hydrocarbon receptor,AhR)的泛素化降解,从而稳定并激活 AhR 信号通路,促进肾脏损伤。与此同时,ApoJ 在肝脏中上调磺基转移酶 1A1(SULT1A1)表达,导致吲哚硫酸(indoxyl sulfate,IS)等尿毒症性色氨酸代谢产物过量生成。肾脏 AhR 信号激活与肝脏毒素过度产生相互协同,形成肝肾互作放大环路,进而加速 CKD 进展。进一步研究发现,肝脏特异性 ApoJ 基因敲除或采用 MK53 多肽靶向抑制 ApoJ,均可显著降低肾脏 AhR 通路活化水平,减少血清吲哚硫酸积累,并有效缓解肾脏损伤。人类肾脏病理样本及患者血清分析进一步验证了上述机制的临床相关性:肾小管及循环系统中 ApoJ 水平升高均与肾损伤程度及尿毒症毒素水平显著相关。
该研究阐明了 ApoJ 通过同时促进肾脏 AhR 信号激活和增强肝脏尿毒症毒素生成,驱动肝肾互作并加速慢性肾病进展,揭示了 CKD 跨器官调控的新机制,并为靶向 ApoJ 的干预策略提供了潜在治疗靶点。
相关成果以 “Apolipoprotein J-mediated hepato-renal crosstalk drives renal injury in chronic kidney disease” 为题发表在国际期刊 Free Radical Biology and Medicine(Q1,IF=8.2)。湖南大学生物学院博士生皮嘉一为论文第一作者,台湾成功大学孙宏羽教授为论文最后通讯作者,湖南大学施李杨教授和广西医科大学段双迪博士为共同通讯作者。
论文链接:https://doi.org/10.1016/j.freeradbiomed.2026.02.018
